Unternehmen im Healthcare-Markt stehen vor einer großen Herausforderung: Sie möchten ihr Angebot durch digitale Lösungen erweitern – müssen dabei aber gleichzeitig eine Vielzahl von regulatorischen Vorgaben und Gesetzen berücksichtigen.
Digitale Lösungen, wie z.B. Medical Apps können die Wirksamkeit von Therapieangeboten und die Adhärenz erhöhen und damit maßgeblich zum Therapieerfolg beitragen. Healthcare-Unternehmen, die Ihr Angebot ausweiten möchten, müssen dabei aber gleichzeitig die nationale und internationale Gesetzgebung zum Datenschutz und zur Datensicherheit berücksichtigen sowie eine Vielzahl von regulatorischen Vorgaben zur Qualitätssicherung, Gebrauchstauglichkeit und Risikobeherrschung. Die Herausforderung ist also groß. Alleine die normenkonforme Dokumentation mit ihrem Aufbau und ihrer Formalistik stellt viele Unternehmen vor eine schier unlösbare Aufgabe.
TWT Health ist nach DIN EN ISO 13485 sowie ISO 27001 zertifiziert und damit für die Entwicklung und den Betrieb von Software und Apps im Gesundheitswesen qualifziert und zugelassen.
Wir können für Sie Software-Projekte gesetzes- und normenkonform planen und entwickeln – und Sie bei Ihrem Entwicklungsvorhaben unterstützen. Das gilt für die Entwicklung von Medizinprodukten genauso wie für Nicht-Medizinprodukte – von der Idee bis zum Launch und darüber hinaus.
Whitepaper: "Medizinische Apps – smarte Helfer oder komplexe Medizinprodukte?"
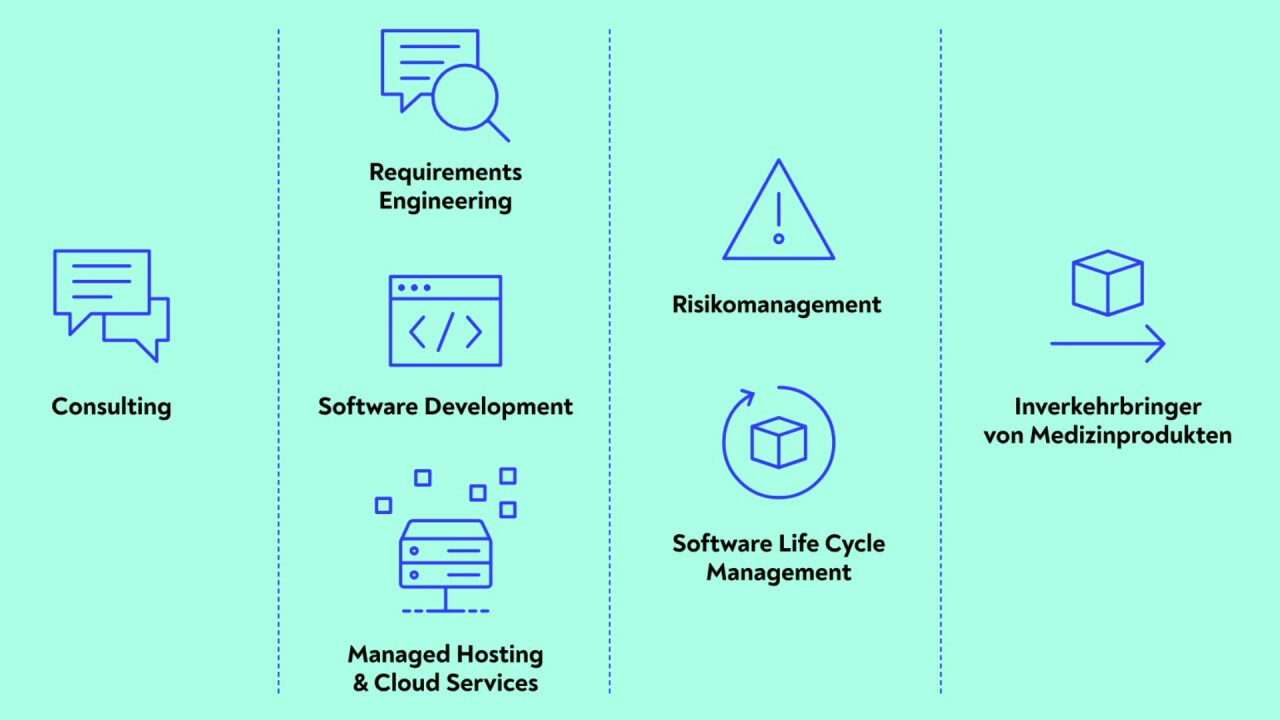
Software als Medizinprodukt entwickeln
Wir planen, entwerfen und implementieren für Sie Software streng nach den Vorgaben der EN IEC 62304 für den Software-Lebenszyklus und der EN IEC 62366 für die Gebrauchstauglichkeit. Dabei dokumentieren wir alle Zwischen- und Endergebnisse in unserem Qualitätsmanagementsystem, welches den Anforderungen der DIN EN ISO 13485 entspricht. Jede Phase der Entwicklung wird durch ein Risikomanagement entsprechend der EN ISO 14971 begleitet, wobei wir unerkannte Gefährdungen bestimmen, das daraus resultierende Risiko bewerten und entsprechende Maßnahmen zur Beherrschung implementieren.
Anforderungen normenkonform erfassen
Gemeinsam mit Ihnen erheben wir die Anforderungen an die Software entsprechend der normativen Vorgaben der EN IEC 62366 in Europa und den USA. Diese sind Voraussetzung für die Durchführung des Software-Lebenszyklus‘ (EN IEC 62304) und der Qualitätssicherung (EN ISO 13485).
Architektur und Design normenkonform planen
Auf der Grundlage der Anforderungen entwerfen wir für Sie die Architektur und das Design Ihrer Software und erstellen Ihnen alle notwendigen Dokumente, wie zum Beispiel die Software-Lebenszyklusakte, die Software-Requirements-Specification (SRS) und die Protokolle der Verifikation und Tests Ihrer Software.
Risiken normenkonform ermitteln, bemessen und beherrschen
Entsprechend der Vorgaben zum Risikomanagement (EN ISO 14971) prüfen wir das Softwarekonzept auf nicht erkannte Gefährdungen, bewerten die Risiken und erarbeiten Beherrschungsmaßnahmen.
Gebrauchstauglichkeit messen und den regulatorischen Vorgaben entsprechend umsetzen
Dank unserer Kooperationspartner können wir die Gebrauchstauglichkeit entsprechend der EN IEC 62366 in Europa und den USA validieren.
Betrieb der Software normenkonform begleiten
Wir begleiten Sie in der nachgelagerten Phase (engl. Post Market Surveillance; PMS) und definieren gemeinsam mit Ihnen die Vigilanz-Prozesse für den Umgang mit unerwünschten Ereignissen.
Notwendige Dokumente für die Konformitätsbewertung einer Medizinprodukte-Software
Wir erstellen alle Dokumente, die für eine Konformitätsbewertung von der MDD bzw. MDR oder von dem FDA CFR gefordert werden. Die gesamte Dokumentation erfolgt in unserem elektronischen Qualitätsmanagementsystem (eQMS), wodurch wir Dokumente, wie die Technische Dokumentation bzw. die Device-Master-Record und die Design-History-File (FDA) automatisch signieren und digital zur Verfügung stellen können. Dabei überprüfen wir die Konformität der Dokumente in einem 6-Augenprinzip und speichern alle Versionsstände nach dem Audit-Trail-Verfahren.
Let's Make Digital Health Happen!
Wir können alle Aufgaben von der Planung über die Entwicklung bis hin zum Betrieb für Sie übernehmen und realisieren Ihre Digital-Health-Idee als Engineering Partner.
Unabhängig davon, ob Sie bereits einen konkreten Plan oder lediglich eine grobe Idee haben – sprechen Sie uns an! Wir freuen uns auf Ihre digitale Herausforderung.
Referenzen und Downloadbereich mit Whitepaper & Case Studies ...